 | |
МЕНЮ
- Главная
- Языкознание филология
- Финансовые науки
- Управленческие науки
- Товароведение
- Технология
- Теплотехника
- Теория организации
- Теория государства и права
- Таможенная система
- Схемотехника
- Строительство
- Страхование
- Статистика
- Религия и мифология
- Психология и педагогика
- Промышленность производство
- Медицинские науки
- Медицина
- Краеведение и этнография
- Компьютерные науки
- История
- Искусство и культура
- Информатика
- Инвестиции
- Издательское дело и полиграфия
- Зоология
- Журналистика
- Естествознание
- Деньги и кредит
- Делопроизводство
- Гражданское право и процесс
- Государство и право
- Геополитика
- Геология
- Геодезия
- География
- Военная кафедра
- Ветеринария
- Валютные отношения
- Бухгалтерский учет и аудит
- Ботаника и сельское хоз-во
- Биржевое дело
- Биология и химия
- Биология
- Безопасность жизнедеятельности
- Банковское дело
- Астрономия
- Астрология
- Архитектура
- Арбитражный процесс
- Административное право
- Авиация и космонавтика
- Карта сайта
Реферат: Технологические основы производства цветных металлов: меди, алюминия, магния, титана
Когда в электролите остается мало глинозема (менее 1%), возникает анодный эффект. Внешне он проявляется в быстром скачке напряжения на электролизере от обычных 4,0-4,7 В до 30-50 В; в области анода появляются электрические дуги, электролит начинает перегреваться и бурлить. Для ликвидации анодного эффекта пробивают корку электролита и, перемешивая, растворяют в нем глинозем (очередная порция которого всегда заранее насыпается на корку электролита).
После растворения глинозема в электролите анодный эффект обычно прекращается и напряжение делается нормальным. Анодный эффект в процессе получения алюминия играет как положительную, так и отрицательную роль. С одной стороны, он сигнализирует о недостатке в электролите глинозема и дает возможность получить представление о ходе электролиза, с другой стороны - он приводит к перерасходу электроэнергии и нарушению теплового равновесия ванны. На заводах стремятся предотвратить частое появление анодных эффектов, вводя глинозем до их появления. В свою очередь, избыток глинозема, введенного в электролит, не растворяется, оседает на дно под слой алюминия, затрудняет нормальный ход электролиза. Поэтому считают нормальным возникновение в электролизере одного-двух анодных эффектов в сутки.
Изучением природы анодного эффекта занималось много исследователей. На основе исследований, проведенных в Московском институте цветных металлов и золота под руководством проф.А.И. Беляева, можно сделать вывод, что причиной, вызывающей анодный эффект, является различная смачиваемость угольного анода расплавленным электролитом при различном содержании в нем окислов. Когда в электролите имеется значительное количество окиси алюминия, электролит хорошо смачивает угольную поверхность анода и поэтому образующиеся анодные газы легко удаляются с его поверхности, не препятствуя прохождению электрического тока. При уменьшении количества глинозема смачиваемость электролитом медленно изменяется и при содержании глинозема менее 1% количество переходит в качество - электролит перестает смачивать угольную поверхность; в результате между электролитом и угольным анодом образуется газовая пленка, препятствующая прохождению электрического тока, что и приводит к резкому повышению напряжения на ванне.
Алюминий извлекают из электролизера, пробивая корку застывшего электролита и опуская на дно футерованную огнеупором стальную трубку, через которую алюминий откачивают в вакуумный ковш. На современной алюминиевой ванне, рассчитанной на силу тока 100 кА, получают в сутки около 700 кг алюминия, поэтому извлечение металла проводят не чаще чем один раз в сутки (из менее мощных ванн один раз за двое суток).
По мере извлечения алюминия анод постепенно опускают, при этом тщательно регулируют напряжение и межполюсное расстояние электролизера. Поскольку нижняя часть анода сгорает и он постепенно опускается, его необходимо наращивать в верхней части. В кожух анода систематически загружают анодную массу, которая коксуется на горячем конусе анода за счет теплоты из ванны. Токоподводящие стальные штыри постепенно опускаются с анодом и во избежание расплавления их поочередно выдергивают из его тела и поднимают на более высокий уровень, а в образовавшуюся полость затекает анодная масса1 и коксуется в ней.
На получение 1 т первичного алюминия электролизом расходуется 15 000-17 000 кВт-ч электроэнергии и почти 2 т глинозема.
Для удаления неметаллических включений (частичек угля, глинозема, фтористых солей и т.д.) извлеченный из электролизеров алюминий часто подвергают 10-15-минутному хлорированию в ковше при температуре 750 °С. Потом алюминий направляют в большие электропечи сопротивления, из которых проводится его полунепрерывная разливка в калиброванные заготовки для производства труб, проволоки и листа (рис.17.8). Эти же печи применяются для получения многих сплавов на алюминиевой основе.
Часть первичного алюминия после отстаивания от примесей в печах САН разливается в чушки на конвейерной машине.
В конце 70-х годов на алюминиевых электролизных заводах СССР резко увеличили объем бесслитковой прокатки листа из расплавленного первичного алюминия. Эти прогрессивные методы значительно экономят труд и электроэнергию, так как отпадает необходимость изготовления слитков, их транспортировки и последующего повторного нагрева. На рис.17.9 показана схема установки для получения алюминиевого листа непосредственно из расплавленного металла.
Первичный алюминий выпускают 13 марок, которые делятся на три группы: алюминий особой чистоты марки А999, четыре марки алюминия высокой чистоты и восемь марок алюминия технической чистоты. В первичном металле допускается содержание примесей от 0,15 до 1,0%, причем название марки указывает на степень чистоты металла. Так, марка алюминия технической чистоты А8 обозначает, что в нем 99,8% алюминия, а примесей (в основном кремния и железа) только 0,2%. В алюминии высокой чистоты марки А99 - соответственно 99,99% алюминия и только 0,01% примесей.
В электролизных ваннах получают алюминий технической чистоты. Для получения алюминия более высоких марок требуется его дополнительное рафинирование.
Глава 3. Производство магния
Магний - серебристо-белый металл. Важнейшее его физическое свойство - малая плотность (р = 1,74 г/см при 20 °С). В электронной оболочке атома магния имеется двенадцать электронов. Два электрона 3s, находящиеся на внешней орбите, легко могут быть оторваны, что приводит к образованию иона Mg'2+, поэтому магний двухвалентен во всех известных соединениях.
Природный магний состоит из смеси трех стабильных изотопов. Причем искусственный изотоп.27Mg с полураспадом 10,2 ч может быть применен в качестве радиоактивного индикатора. Кристаллы магния обладают компактной гексагональной структурой.
При хранении магния на сухом воздухе на его поверхности образуется окисная пленка, предохраняющая металл при небольшом нагревании (до 200 °С) от дальнейшего окисления; в этих условиях коррозионная стойкость чистого магния превышает стойкость низкоуглеродистой стали. Однако во влажном воздухе его коррозия значительно усиливается. На него практически не действует керосин, бензин и минеральные масла. Однако он не стоек в водных растворах солей (кроме фтористых) и растворяется во многих минеральных и органических кислотах.
Магний в виде слитков или изделий не огнеопасен. Возгорание магния может произойти лишь при температуре, близкой к точке его плавления (651 °С) или после расплавления, если он не изолирован от кислорода воздуха. Покрытый флюсом, металл можно нагребать и плавить. Порошкообразный магний или тонкая магниевая лента легко загорается от спички и горит ослепительно белым пламенем. Магний немагнитен и не искрит при ударах пли трении.
В свободном виде он не встречается, но входит в виде карбонатов, силикатов в состав многих горных пород, а также растворен в морской и озерной воде в виде хлоридов и сульфатов.
В настоящее время для получения магния применяют магнезит, доломит, карналлит, а также морскую воду и отходы ряда производств.
Природный минерал магнезит кроме карбоната магния MgC03 обычно содержит карбонат кальция, кварц, а также примеси других минералов, включающих окислы алюминия и железа. Для производства магния применяют только чистый каустический магнезит, полученный по реакции MgC03 = MgO + CO2 при нагревании (обжиге) природного магнезита до 700-900 °С.
Доломит - горная порода, представляющая собой двойной карбонат кальция и магния MgC03-СаС03. Доломиты обычно содержат примеси кварца, кальцита, гипса и др. Содержание и окраска примесей определяют цвет породы. Доломит широко распространен в природе и составляет около 0,1% всех горных пород, входящих в состав земной коры. Доломит, так же как и магнезит, предварительно обжигают до получения смеси окислов MgO и СаО.
Карналлит - природный хлорид магния и калия - очень гигроскопичное кристаллическое вещество, обычно окрашенное примесями в розовый, желтый пли серый цвет. Карналлит подвергают гидрохимической обработке для выделения из него брома и некоторого количества хлористого натрия и калия, в результате чего получается так называемый искусственный карналлит, который применяется в магниевой промышленности.
Неисчерпаемы запасы магния в виде бишофита MgCl2 * 6Н,0 в морской воде; в среднем там содержится 0,38% MgCl2. Кроме того, в морской воде имеются соединения магния MgS04 (0,17%) и MgBr2 (0,01%).
Морская вода пока редко используется для получения бишофита, так как во многих странах имеются соляные озера, в воде которых содержание хлористого магния значительно выше. В некоторых озеpax перекопской группы, например, содержание хлористого магния к концу лета достигает 15%. Кроме того, сырьем для получения магния теперь служат отходы ряда производств. При этом особенно, широко используют хлористый магний, получаемый при извлечении титана из его руд.
Понятие об электролитической способе получения магния. В основном магний получают электролитическим способом, важнейшими стадиями которого являются: а) получение чистых безводных солей магния; б) электролиз расплава этих солей и в) рафинирование магния.
Варианты электролитического способа получения магния различаются по составу солей, поступающих на электролиз (карналлит, хлористый магний и т.д.), и по способу получения этих солей (хлорирование магнезита, обезвоживание бишофита или карналлита). Хлорирование магнезита можно проводить аналогично хлорированию окиси титана. Обезвоживание карналлита обычно проводят в две стадии: вначале медленным нагреванием природного карналлита в трубчатых печах, а затем плавлением соединения КCl* MgCl2 * Н20 до полного удаления гидратной влаги.
Электролиз проводят в расплавленных хлоридах магния, калия, натрия и кальция, так как при электролизе водных растворов его солей из-за отрицательного потенциала магния на катоде выделяется только водород.
Схема электролизера для получения магния изображена на рисунке:

Электролизер для получения магния.
Анодами служат графитные плиты 4, катодами - стальные пластины 2. Так как плотность расплавленного электролита больше, чем плотность магния в этих же температурных условиях, то выделяющийся на катоде жидкий магний, не растворяясь в электролите, в виде капель всплывает на поверхность. На аноде выделяется газообразный хлоp, который также поднимается и выбрасывается из электролита. Во избежание взаимодействия хлора и магния и короткого замыкания анода и катода расплавленным магнием вверху устанавливают перегородку 1, которую принято называть диафрагмой. Во время электролиза расходуется хлористый магний, периодически вводимый в электролит.
Собирающийся на поверхности катодного пространства магний периодически удаляют. Выделяющийся в анодном пространстве хлор всасывают через трубы 3 и используют, например, для хлорирования окиси магния или окиси титана.
Магний можно получить электролизом чистого расплавленного безводного хлористого магния, однако высокая температура плавления, низкая электропроводность и другие неблагоприятные свойства этой соли вынуждают прибегать к электролитам более сложного состава. Практически удобнее вести электролиз карналлита, который обычно содержит в виде примеси хлористый натрий. Такой электролит обладает более низкой температурой плавления, более высокой электропроводностью и меньше растворяет магний. Поэтому при работе с ним достигается меньший расход электроэнергии.
Магниевые ванны соединяются между собой последовательно в серии по 60-100 шт. Число ванн в серии определяется напряжением источника постоянного электрического тока; напряжение ванны, которое зависит от ее конструкции, межполюсного расстояния, состава электролита, колеблется в пределах 5,5-7,5 В.
Обслуживание ванн заключается в выполнении следующих основных операций: а) питании электролитом; б) регулировании температуры; в) извлечении магния; г) удалении шлама.
Питание ванн электролитом. В процессе электролиза идет непрерывное разложение хлористого магния, поэтому для восполнения го расхода в ванну периодически вводят свежие расплавленные мористые соли. Наиболее удобно добавлять в электролит безводный Хлористый магний, получающийся при восстановлении хлорида титана магнием. В случае автономного расположения магниевого завода бишофит приходится предварительно обезвоживать. Можно вводить в ванну и безводный карналлит, но тогда необходимо сливать часть электролита, так как иначе в нем будет избыток хлорида калия. Из отработанного электролита получают калийные удобрения.
Регулирование температуры. Электролиз должен протекать при температуре 690-720 °С, при этом нижнего предела желательно придерживаться при питании ванн хлористым магнием, а верхнего - при питании карналлитом. В процессе электролиза необходимо наблюдать за температурой электролита, так как отклонение от нормы, особенно в сторону повышения, значительно ухудшает показатели Iпроцесса.
В магниевых ваннах для регулирования температуры не меняют межполюсное расстояние, как это принято при электролитическом получении алюминия, а изменяют состав, а с ним и электропроводность электролита. Так, например, чтобы поднять температуру электролита, следует залить в него больше чистого хлористого магния, что увеличит сопротивление электролита. Изменения температуры в пределах 20-30 °С можно добиться, варьируя количество отсасываемых газов из катодного пространства ванны.
В случае перегрева электролита применяют загрузку твердого хлористого натрия; при чрезмерном падении температуры, например при выключении ванны, используют подогрев электролита переменным током, опуская в катодные ячейки нихромовые спирали.
Извлечение магния из электролизера. Это обычно производят не реже одного раза в сутки, применяя вакуумные ковши. Ковш предварительно нагревается вмонтированными в него нагревательными элементами и затем подается к ваннам мостовым краном. После создания в нем разрежения 730-800 кПа в ячейку ванны опускают всасывающую трубу и открывают клапан. Металл и часть электролита засасываются в ковш. Затем клапан закрывают и повторяют операцию в других ячейках ванны.
Удаление шлама. В электролит с хлористым магнием поступает и окись магния; кроме того, может протекать гидролиз электролита с образованием окиси магния. Она оседает на дно электролизера, увлекая за собой другие продукты и образуя шлам. Шлам удаляют один раз в два-три дня, не допуская значительного накопления его на дне ванны, так как это иногда приводит к замыканию анода с катодом и ухудшает условия осаждения магния на катоде.
Глава 4. Производство титана
Титан получают магнийтермическим способом, сущность которого состоит в обогащении титановых руд, выплавке из них титанового шлака с последующим получением из него четыреххлористого титана и восстановлении из последнего металлического титана магнием.
Сырьем для получения титана являются титаномагнетитовые руды, из которых выделяют ильменитовый концентрат, содержащий 40-45% TiO2, ~30% FeO, 20% Fe2O3 и 5-7% пустой породы. Название этот концентрат получил по наличию в нем минерала ильменита FeО*TiO2.
Ильменитовый концентрат плавят в смеси с древесным углем, антрацитом в рудно-термических печах, где оксиды железа и титана восстанавливаются.
Образующееся железо науглероживается, и получается чугун, а низшие оксиды титана переходят в шлак. Чугун и шлак разливают отдельно в изложницы.
Основной продукт этого процесса-титановый шлак. Побочный продукт этого процесса - чугун используют в металлургическом производстве. Полученный титановый шлак подвергают хлорированию в специальных печах. В нижней части печи располагают угольную насадку, нагревающуюся при пропускании через нее электрического тока. В печь подают брикеты титанового шлака, а через фурмы внутрь печи-хлор. При температуре 800 - 1250° С в присутствии углерода образуется четыреххлористый титан, а также хлориды.
Четыреххлористый титан отделяется и очищается от остальных хлоридов благодаря различию температуры кипения этих хлоридов методом ректификации в специальных установках.
Титан из четыреххлористого титана восстанавливают в реакторах при температуре 950-1000° С. В реактор загружают чушковый магний; после откачки воздуха и заполнения полости реактора аргоном внутрь его подают парообразный четыреххлористый титан. Между жидким магнием и четыреххлористым титаном происходит реакция 2Mg+TiCl4=Ti+2MgCl2.
Твердые частицы титана спекаются в пористую массу-губку, а жидкий MgCl2 выпускают через летку реактора. Титановая губка содержит 35-40% магния и хлористого магния.
Для удаления из титановой губки этих примесей ее нагревают до температуры 900-950° С в вакууме. Титановую губку плавят методом вакуумно-дугового переплава.
Вакуум в печи предохраняет титан от окисления и способствует очистке его от примесей. Полученные слитки титана имеют дефекты, поэтому их вторично переплавляют, используя как расходуемые электроды. После этого чистота титана составляет 99,6 - 99,7%. После вторичного переплава слитки используют для обработки давлением.
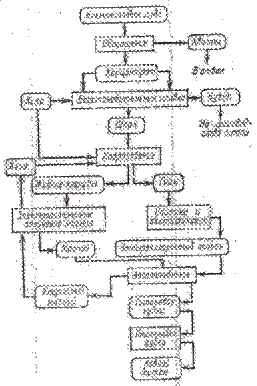
Упрощенная схема получения титана
Заключение
Подводя итоги, можно сделать следующий вывод: в настоящее время цветные металлы и сплавы на их основе находят весьма широкое применение. Наибольшее применение получили сплавы на основе меди, алюминия, магния. Указанные металлы в чистом виде в промышленности не применяют, но технически чистые, содержащие небольшое количество примесей, используют достаточно часто.
Медь выпускают в виде листов, лент нормальной и повышенной точности, проволоки, прутков разного сечения. Медь является основой важнейших сплавов - латуней и бронз. Сплавы меди с цинком называют латунями, а сплавы со всеми другими элементами - оловом, алюминием, бериллием и др. - бронзами.
Широко используются в народном хозяйстве сплавы меди с никелем - мелъхиоры, иногда с небольшими добавками железа и марганца, а также меди с цинком и никелем (иногда с добавлением кобальта) - нейзильберы. Мельхиоры отличаются высокой химической стойкостью в морской воде, растворах солей, органических кислотах, они весьма пластичны. Их применяют в морском судостроении, для изготовления разменной монеты, медицинского инструмента, деталей аппаратуры точной механики и др. Нейзильберы обладают высокими прочностью и коррозионной стойкостью. Они используются в производстве точных приборов, часов и т.д.
Алюминий. Благодаря ряду положительных свойств алюминия и большого количества его в земной коре (до 7,45%) он широко применяется в производстве в виде различных сплавов. Чистый алюминий из-за высокой химической активности в природе не встречается и в технике не применяется.
Алюминий - мягкий металл серебристо-белого цвета. Имеет высокие электро- и теплопроводность, большую скрытую теплоту плавления. Технически чистый алюминий выпускается нескольких марок и применяется в основном для изготовления радиоэлектронной аппаратуры (электролитических конденсаторов, фольги и др.). Сплавы алюминия применяются практически во всех отраслях промышленности (авиационной, ракетостроительной, приборостроительной и др.). Наибольшее применение имеют сплавы алюминия с кремнием, магнием и медью (литейные и деформируемые).
Лучшим деформируемым сплавов на алюминиево-медной основе является дюралюминий. Дюралюминий, имея малую плотность (2,85 г/см3), обладает высокими механическими свойствами, не уступающими свойствам низкоуглеродистых сталей. Свойства дюралюминия повышаются с проведением закалки и старения сплава.
Лучшими литейными сплавами являются силумины (на основе алюминий - кремний), из которых изготовляют детали различных приборов и радиоаппаратов, корпуса турбонасосных агрегатов и др.
Магний быстро окисляется на воздухе, имеет весьма низкие механические свойства. Поэтому как конструкционный материал он не применяется, а вводится в качестве компонента в сплавы. Магниевые сплавы делятся на деформируемые и литейные. Широкое применение магниевого литья объясняется, в частности, малой плотностью магния, что обеспечивает получение деталей малой массы.
Титан - малопрочный серебристо-серый металл. В чистом виде в технике не применяется. Введение в титан различных компонентов позволяет получать требуемые свойства сплавов.
Применяют также литейные титановые сплавы, обеспечивающие высокую плотность отливок. Эти сплавы дают малую линейную усадку, не подвержены образованию трещин в горячем состоянии, что позволяет изготовлять отливки сложной формы.
Плавка и разливка титановых сплавов производится в защитной атмосфере и вакууме.
Список использованной литературы
1. Кузьмин Б.А., Самохоцкий А.И. Металлургия, металловедение и конструкционные материалы: учебник для механических и машиностроительных техникумов, М.: Высшая школа, 1984
2. Браун Д.А., Разыграев А.М. Технология металлов и конструкционные материалы, М.: Высшая школа, 1965
3. Технология металлов и других конструкционных материалов под ред. проф. Дубинина Н.П., М.: Высшая школа, 1969
4. Архипов В.В., Касенко М.А., Ларин М.Н. и др. Технология металлов, М.: Высшая школа, 1964
5. Никифоров В.М. Технология металлов и конструкционные материалы: учебник для средних специальных учебных заведений, Л.: Машиностроение, Ленинградское отделение, 1986.