 | |
МЕНЮ
- Главная
- Языкознание филология
- Финансовые науки
- Управленческие науки
- Товароведение
- Технология
- Теплотехника
- Теория организации
- Теория государства и права
- Таможенная система
- Схемотехника
- Строительство
- Страхование
- Статистика
- Религия и мифология
- Психология и педагогика
- Промышленность производство
- Медицинские науки
- Медицина
- Краеведение и этнография
- Компьютерные науки
- История
- Искусство и культура
- Информатика
- Инвестиции
- Издательское дело и полиграфия
- Зоология
- Журналистика
- Естествознание
- Деньги и кредит
- Делопроизводство
- Гражданское право и процесс
- Государство и право
- Геополитика
- Геология
- Геодезия
- География
- Военная кафедра
- Ветеринария
- Валютные отношения
- Бухгалтерский учет и аудит
- Ботаника и сельское хоз-во
- Биржевое дело
- Биология и химия
- Биология
- Безопасность жизнедеятельности
- Банковское дело
- Астрономия
- Астрология
- Архитектура
- Арбитражный процесс
- Административное право
- Авиация и космонавтика
- Карта сайта
Курсовая работа: Получение ферментных препаратов выращенных глубинным способом
Наиболее широким и перспективным источником протеиназ являются микроорганизмы. Активными продуцентами протеиназ являются бактерии, микроскопические грибы и актиномицеты. Можно назвать сотни микроорганизмов, принадлежащих к различным таксономическим группам, которые используются при промышленном получении протеиназ. Они чаще всего относятся к родам Bacillus, Aspergillus, Penicillium, Streptomyces, Pseudomonas и некоторые другие. Более подробно о продуцентах будет сказано в разделе, посвященном рассмотрению особенностей производства протеолитических препаратов.
2.2 Механизм действия, свойства и классификация протеиназ
Субстрат. Субстратами для действия протеолитических ферментов являются пептиды и белки. К последним относятся простые белки, состоящие только из аминокислот, их называют протеинами, и сложные белки, в состав которых наряду с белковой частью молекулы входят соединения небелковой природы (углеводы, витамины, жиры и др.) – протеиды. Все эти соединения имеют большую молекулярную массу и сложны по строению.
Пептиды также могут быть субстратом для протеиназ. Они имеют более низкую молекулярную массу, чем белки, и по составу подобны простым белкам. Они могут быть либо продуктами неполного гидролиза белка, либо природными соединениями. Пептиды могут быть синтезированы в лаборатории и использоваться как специфические субстраты в аналитических работах для определения способности ферментов к разрыву вполне определенных пептидных связей.
До начала 50-х годов все протеолитические ферменты по механизму их действия на субстрат подразделялись на две группы: протеиназы и пептидазы. Считалось, что гидролиз белка протекает в две стадии: сначала под действием протеиназ белки гидролизуются до пептидов, а затем на пептиды действуют пептидазы и расщепляют их до аминокислот.
Позднее, в 60-х годах, протеолитические ферменты классифицировали на четыре подкласса. В настоящее время действует новая классификация, по которой протеиназы относятся к третьему классу четвертому подклассу. С тем чтобы исключить путаницу, все ранее существовавшие подклассы были отброшены и по новой классификации первому подклассу в разделе протеолитических ферментов присвоен номер 11 (КФ 3.4.11). Такие сложности в классификации связаны с тем, что катализируемая суммарная реакция одинакова для всех протеолитических ферментов. Причем ферменты не имеют строгой субстратной специфичности в обычном смысле этого слова – подавляющее большинство этих ферментов действует на все денатурированные и на многие нативные белки. По новой классификации протеолитические ферменты были разделены на две основные группы: пептидазы КФ 3.4.11 – 15 и протеиназы – КФ 3.4.21 – 24.
Пептидазы. В первой группе протеолитических ферментов – пептидазах – подразделение по подподклассам осуществляется на основе механизма расщепления пептидных связей в пептидах. К группе ферментов, входящих в 11-й подподкласс (КФ 3.4.11) – α-аминоацилпептидгидролазы – относятся те, которые гидролитически расщепляют первую с N-конца пептидную связь. Группа КФ 3.4.12 – гидролазы пептидиламинокислот или гидролазы ациламинокислот – объединяет ферменты, действующие на первую пептидную связь с С-конца. Ферменты группы КФ 3.4.13 – дипептидгидролазы – гидролизуют дипептиды; групп КФ 3.4.14 – дипептидилпептид гидролазы – и КФ 3.4.15 – пептидилдипептидгидролазы – гидролизуют дипептиды соответственно с N- и С-конца. С 16-го до 20-го подподкласса в номенклатуре сделан пропуск с учетом будущих открытий ферментов, гидролизующих дипептиды.
Протеиназы. Вторая группа протеолитических ферментов – протеиназы – имеет четыре подподкласса (21 – 24), в котором все ферменты подразделяются в зависимости от особенностей механизма катализа, установленного по функционированию активного центра фермента, а также влияния рН на его активность. Специфичность к субстрату рассматривается лишь с позиции идентификации индивидуальных ферментов в пределах каждой из групп.
Сериновые протеиназы. К подподклассу 3.4.21 относятся протеиназы, для которых характерно наличие в каталитическом центре триады аминокислот: аспарагиновая кислота, гистидин и серии. В этот подподкласс внесены многие хорошо изученные протеийазы животного происхождения (химотрипсин, трипсин, тромбин, плазмин, эластаза и др.) и некоторые микробные протеиназы.
Тиоловые протеиназы. К подподклассу 3.4.22 относятся протеиназы, имеющие в активном центре SH-группу цистеина.
В подподкласс 3.4.22 вошел ряд важных протеиназ растительного происхождения, такие как папаин, фицин, бромелаин, химопапаин, и некоторые микробные протеиназы.
Кислые протеиназы. Они входят в подподкласс (3.4.23) и имеют оптимальный рН ниже 5, в каталитическом акте у этих ферментов участвуют остатки дикарбоновых аминокислот. Наиболее широко известны из этого подподкласса пепсин, катепсин и ряд кислых протеиназ грибного происхождения. В последний под подкласс (3.4.24) входят протеиназы, содержащие ионы металлов. В основном это различные микробные нейтральные протеиназы и некоторые протеиназы животного происхождения.
В классификации и номенклатуре протеолитических ферментов выделена ещё одна, третья группа протеиназ, которые включены в подподкласс 3.4.99. Это протеиназы с неизвестным механизмом катализа. В этот подподкласс внесено 26 ферментов, среди них много микробных протеиназ, но есть протеиназы и животного происхождения. Создание подподкласса 3.4.99 вызвано тем, что многие протеиназы обладают близкой, но не полностью изученной и определенной специфичностью. Они действуют на один и тот же субстрат, однако продукты гидролиза отличаются не только количественно, но и качественно.
Отличительной особенностью многих протеолитических ферментов животного происхождения является то, что они в организме существуют в неактивном состоянии в виде зимогенов, которые только при определенных условиях могут превращаться в активные формы. Это трипсин, химотрипсин, карбоксипептидазы, А и В, пепсины, реннин, катепсины, аминопептидазы, дипептидазы, тромбин, плазмин и др. Многие из данных ферментов получены в кристаллическом виде. Они чаще используются в медицине. Механизм их действия, субстратная специфичность, механизм ингибирования и активации подробно изучены. Имеются данные о строении активного центра, а для некоторых протеиназ известна и структура самого фермента. Также глубоко и всесторонне изучены основные протеиназы растительного происхождения: папаин, фицин, бромелаин, химопапаин, которые за рубежом широко применяются в медицине и пищевой технологии.
2.3 Получение микробных протеиназ
В Номенклатуру и классификацию ферментов внесено большое количество протеолитических ферментов микробного происхождения, которые относятся к различным подподклассам: 3.4.11 (7 ферментов), 3.4.13(5), 3.4.15(1), 3.4.16(1), 3.4.17(5), 3.4.21(4), 3.4.22(3), 3.4.23(1), 3.4.24(4) и 3.4.99(4). Необходимо отметить, что часто под одним номером находится очень много ферментов, получаемых из различных источников, но имеющих сходные свойства. Так, в подподклассе 3.4.21.14 представлена целая серия микробных протеиназ, среди продуцентов которых отмечаются Bacillus subtilis, E. coli, щелочная протеиназа из культур рода Aspergillus, Tritirachium album, Arthrobacter, Pseudomonas aeruginosa, Malbranchea pulchella, Streptomycer rectus, Candida lipolytica и др. Под номером 3.4.23.6 также объединено много ферментов, источниками которых являются микроорганизмы, в основном относящиеся к грибам родов: A. oryzae, A. terricola, A. saitoi, A. niger, P. janthinellum, R. chinensis, M. pusillus, M. miehei, Endothia parasitica, Candida albicans, Saccharomyces carlsbergensis, Rhodotorula glutinis, Physarum polycephalum и др. Все микробные металлопротеиназы объединены под номером 3.4.24.4. Они выделены из культур родов: Streptomyces, Sarcina, Micrococcus, Staphylococcus, Bacillus, Aeromonas, Pseudomonas, Escherichia, Aspergillus, Myxobacter, Serratia.
Однако в промышленности чаще всего получают комплекс протеолитических ферментов, достоинства которого определяются с учетом последующего применения ферментного препарата. Суммарная протеолитическая активность такого препарата определяется на соответствующем субстрате: гемоглобине, желатине, растительном белке, эластине, коллагене и т. д.
2.3.1 Технологические схемы производства микробных протеиназ
Технологические схемы производства микробных протеиназ (см. рис. 1 и 5) отличаются друг от друга прежде всего на первой стадии получения микробной культуры продуцента, на стадиях выделения различия меньше.
2.3.2 Продуценты
В качестве продуцентов протеолитических ферментов при глубинном культивировании в промышленных условиях используют бактерии в основном рода Bacillus, реже – актиномицеты и микроскопические грибы. Способность к образованию протеолитических ферментов отмечается практически у всех известных микроорганизмов, так как роль этих ферментов в регуляции жизненных функций организмов очень велика. Протеолитические ферменты в подавляющем большинстве случаев являются внеклеточными.
2.3.3 Регуляция синтеза протеиназ
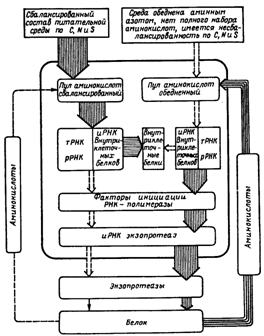
В самом общем виде гипотетический механизм регуляции биосинтеза внеклеточных протеаз у микроорганизмов представлен на рисунке 14. Авторы этой модели, основываясь на данных литературы и собственных исследованиях, предполагают, что иРНК-экзопротеазосинтезирующая система безуспешно конкурирует с системами других РНК вследствие низкого сродства специфических факторов инициации или РНК-полимеразы с участком инициации на экзобелковом гене. Известно, что синтез РНК контролируется либо соотношением ненагруженных и аминоацилированных тРНК (при этом свободные тРНК являются репрессорами синтеза), либо действием гуанозинтетрафосфата (ppGpp), который образуется при аминокислотном голодании и подавляет биосинтез РНК. Суть предлагаемой модели заключается в следующем. Присутствие в среде в достаточном количестве всех необходимых аминокислот и других источников углерода, азота и серы позволяет поддерживать внутриклеточный пул микроорганизма на высоком уровне. При этих условиях клетка осуществляет интенсивный синтез нетранслируемых РНК и иРНК для внутриклеточных белков. В результате содержание свободных факторов инициации РНК-полимеразы, которые могут принять участие в синтезе иРНК экзопротеаз, незначительно. Вероятно, этим объясняется низкая частота транскрипции иРНК экзопротеаз и, следовательно, низкий уровень образования внеклеточных протеаз, например, в начале роста культуры на такой сбалансированной среде (левая сторона схемы).
Истощение среды в процессе роста культуры по одному или нескольким субстратам приводит к снижению уровня пула внутриклеточных свободных аминокислот, что значительно снижает синтез РНК. В результате освобождаются РНК-полимераза и факторы инициации транскрипции РНК. Увеличиваются частота инициации иРНК экзопротеаз и соответственно синтез внеклеточных протеолитических ферментов (правая сторона схемы). При наличии в среде белков экзопротеазы расщепляют их до пептидов и аминокислот, которые поступают в клетку, пополняя ее пул. Аминокислоты утилизируются клеткой активно и являются лимитирующим субстратом. Поступающие в клетку аминокислоты могут полностью удовлетворить ее потребности, т. е. снять лимитирование по этому субстрату, что приведет к временному торможению биосинтеза экзопротеаз и т. д. Иными словами, имеет место механизм контроля синтеза экзопротеаз по типу метаболитной репрессии. Можно предположить, что регуляторное воздействие субстратов на биосинтез экзопротеаз проявляется на уровне транскрипции. Известно, что пул иРНК поддерживает синтез протеаз в течение нескольких часов.
Глубинным способом культивируют многие продуценты протеолитических ферментов. Для производства нейтральных и щелочных протеиназ используют спороносные бактерии и актиномицеты, для получения кислых – микроскопические грибы.
Наиболее широко в нашей стране применяются штаммы бактерий, относящиеся к видам Bacillus subtilis и В. mesentericus, на основе которых выпускаются препараты протосубтилин и протомезентерин разной степени очистки, предназначенные для самых различных отраслей – от пищевых технологий до использования в моющих средствах и сельском хозяйстве.
2.3.4 Питательные среды и условия культивирования
При конструировании оптимальных питательных сред для каждого продуцента изучаются его физиология, потребность в источниках N, С и других соединениях. Содержание сухого вещества в питательной среде в зависимости от продуцента может изменяться от 6 до 20 %. Питательные вещества могут вноситься в среду сразу или дробно по мере потребления из среды лимитирующего компонента. Оптимальный состав среды устанавливается либо путем длительного изучения особенностей биосинтеза ферментов микроорганизмом, либо с использованием математических методов планирования эксперимента.
Способ экспериментального конструирования питательной среды можно продемонстрировать на примере Bacillus subtilis 103 (табл. 3,).
|
Таблица 3 |
||||
| Источник азота | рН | Содержание биомассы, г на 100 мл | Протеолитическая активность, мкг тирозина на 1 мл | |
| начальный | конечный | |||
| Цитрат аммония двузамещённый (контроль) | 6,90 | 7,50 | 0,84 | 66,8 |
| KN03 | 6,90 | 6,10 | 0,11 | 97,0 |
| NH4NO3 | 6,90 | 4,45 | 0,26 | 0 |
| (NH4)S04 | 6,90 | 4,80 | 0,40 | 66,8 |
| (NH4)2HP04 | 6,90 | 5,60 | 0,80 | 100,2 |
| NH4Cl | 6,95 | 7,40 | 0,40 | 67,0 |
| Двузамещённый фосфат аммония (контроль) | 6,9 | 5,6 | 0,80 | 100,2 |
| Казеин | 6,9 | 7,7 | 0,80 | 140,0 |
| Пептон | 6,9 | 7,5 | 1,00 | 187,7 |
| Кукурузный экстракт | 6,8 | 7,6 | 1,00 | 200,0 |
| Глютен | 7,0 | 6,8 | 0,74 | 56,8 |
| Вытяжка из солодовых ростков | 7,0 | 7,3 | 0,60 | 193,7 |
Культивирование проводилось на модифицированной среде Номура следующего состава (в %): картофельный крахмал – 2; двузамещённый цитрат аммония – 3; КСl – 0,15; MgSO4 – 0,05; СаС12 – 0,01; экстракт соевых бобов – 1,0. Если в составе среды изменять источник минерального азота (см. табл. 2.37), то биосинтез протеолитических ферментов будет заметно изменяться, особенно, если соль кислая, например NH4NO3. При потреблении аммонийного азота в среде накапливаются ионы азотной кислоты и среда резко подкисляется, и, хотя рост культуры и происходит, биосинтеза протеиназ не наблюдается. Если взять двузамёщенный фосфат аммония за контроль, то при изучении влияния различных источников органического азота для этого же штамма (табл. 4) оказалось, что уровень рН меняется меньше, чем с неорганическим азотом, и только в одном случае – с глютеном – биосинтез протеолитических ферментов ниже контрольного. Кроме того, введение в состав среды помимо (NH4)2HPO4 (1,2 %) кукурузного экстракта (0,8 %) и пивных дрожжей (0,4 %) позволило получить активность в культуральной жидкости до 1 300 ед. ПС/мл, т. е. почти в 20 раз больше контроля.
ИНТЕРЕСНОЕ
© 2009 Все права защищены. |