 | |
МЕНЮ
- Главная
- Языкознание филология
- Финансовые науки
- Управленческие науки
- Товароведение
- Технология
- Теплотехника
- Теория организации
- Теория государства и права
- Таможенная система
- Схемотехника
- Строительство
- Страхование
- Статистика
- Религия и мифология
- Психология и педагогика
- Промышленность производство
- Медицинские науки
- Медицина
- Краеведение и этнография
- Компьютерные науки
- История
- Искусство и культура
- Информатика
- Инвестиции
- Издательское дело и полиграфия
- Зоология
- Журналистика
- Естествознание
- Деньги и кредит
- Делопроизводство
- Гражданское право и процесс
- Государство и право
- Геополитика
- Геология
- Геодезия
- География
- Военная кафедра
- Ветеринария
- Валютные отношения
- Бухгалтерский учет и аудит
- Ботаника и сельское хоз-во
- Биржевое дело
- Биология и химия
- Биология
- Безопасность жизнедеятельности
- Банковское дело
- Астрономия
- Астрология
- Архитектура
- Арбитражный процесс
- Административное право
- Авиация и космонавтика
- Карта сайта
Курсовая работа: Розвиток творчої активності школярів у процесі розв’язування розрахункових задач з хімії
Системність в розв’язку задач передбачає, що кожна наступна задача повинна мати конкретну новизну, бути посильно важкою, потребувати відповідних прийомів праці над нею.
При системному підході до курсу хімії теоретичні знанні і вміння розв’язувати задачі складають єдину систему хімічних знань, яка забезпечує поглиблене і зрозуміле засвоєння знань учнями одночасно з оволодінням структурою самих задач.
У процесі розв’язування задач відбувається уточнення і закріплення хімічних понять про речовини і процеси. Задачі, які включають визначені ситуації, стають стимулом самостійної роботи учнів над навчальним матеріалом. Стає зрозумілою загальноприйнята в методиці думка, що мірою засвоєння матеріалу потрібно вважати не тільки і навіть не скільки переказ тексту підручника, скільки умінню використовувати одержані знання при розв’язуванні різноманітних задач.
Тісна взаємодія знань і умінь являється основою формування різноманітних прийомів мислення: доведення, судження і умовиводів. У свою чергу знання, які використовують при розв’язуванні задач можна розділити на два типи: знання, які учень набуває при розборі тексту задачі і знання, без використання яких процес розв’язку неможливий. Сюди належать різноманітні визначення, знання основних теорій і законів, різні хімічні поняття, фізичні і хімічні властивості речовин, формули сполук, рівняння хімічних реакцій і т.д. психологи і дидакти розглядають розв’язування задач як модель комплексу розумових дій. Мислення при цьому виступає як проблема “складання” операцій в конкретну систему знань з її послідуючим узагальненням.
Значна роль задач в організації пошукових ситуацій, які необхідні при проблемному навчанні, а також в процесі перевірки знань учнів, при закріпленні отриманого на уроці матеріалу.
Для виявлення функцій, ролі і місця хімічних задач у системі методів навчання, рівня засвоєння учнями навчального матеріалу, розвитку пізнавальних здібностей і творчих можливостей учнів задачі класифікують за різноманітними ознаками. У підручниках з методики хімії (Н.М. Буринська, Г.М. Чернобельська, О.С. Зайцев), спеціальних методичних посібниках по розв’язуванню задач і в інших виданнях приводяться різноманітні варіанти класифікації задач. Загальновизнаною є класифікація на дві групи:
– розрахункові;
– якісні.
При розв’язуванні якісних задач визначаються якісні співвідношення між хімічними поняттями. При розв’язуванні кількісних задач – кількісну залежність між даними і шуканим. Щоб отримати відповідь на кількісну задачу, потрібно провести конкретні математичні операції. Початковим етапом розв’язку розрахункових задач є якісний аналіз, який доповнюється кількісним.
Д.П. Єригін і Є.А. Шишкін умовно поділяють хімічні розрахункові задачі на три групи:
1. Задачі, які розв’язуються з використанням хімічної формули речовини або на виведення формули;
2. Задачі, для розв’язання яких використовують рівняння хімічних реакцій;
3. Задачі, які пов’язані з розчинами речовин.
У методичній літературі і в програмах шкільного курсу хімії задачі в основному класифікуються за способами розв’язування. Пропонуємо таку класифікацію для визначення місця задач у навчальному процесі (схема 2).
Схема 2

Кожна з груп включає різноманітні типи задач (схема 3).
Різноманітність типів задач, які отримані авторами – Шаповаленко С.Г., Шевальовою А.С., Плентером Ю.В. і Полосіним В.С. – Єригін Д.П і Шишкін Є.А. оформили у вигляді таблиці (таблиця 2).
Коли навчаєш хімії, на практиці, часто бувають випадки, коли кількісні задачі розв’язуються без достатнього якісного аналізу, підстановкою даних в пропорцію або формулу, які підбираються за допомогою формальних властивостей. При цьому, на перший план виступають математичні операції, які перекривають хімічну суть задачі.
Схема 3
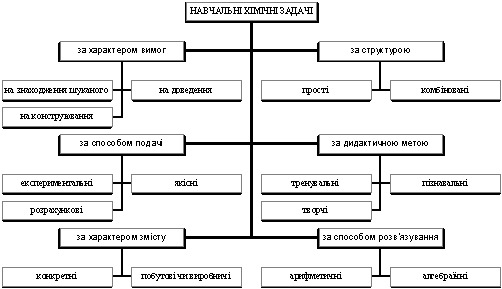
За психологічними дослідженнями розв’язування хімічних задач досить часто ускладнюється великим розрахунковим апаратом, який створює видимість розумових зусиль, а насправді, штучно утримує використання активних форм розумової діяльності учнів. Захоплення математичними розрахунками під час розв’язку хімічних задач призводить до того, що хімічна суть переходить на другий план. Внаслідок цього друга сигнальна система, яка функціонує під час визначення словесними і математичними формулами не знаходить достатньої опори у першій сигнальній системі, а отже , – і в фактах дійсності.
Тільки це і дало можливість М.В. Зуєвій зробити висновки про незначну методичну цінність розрахункових хімічних задач.
Таблиця 2 Класифікація задач за типами, які запропоновані різними методистами
| Шаповаленко С.Г. | Шевальова А.С. | Плетнер Ю.В, Полосін В.С. |
| 1. Ознайомлення з хімічною мірою маси, “моль”. | 1. Розрахунки за формулами. | 1. Розрахунки за формулами. |
| 2. Розрахунки за хімічною формулою співвідношень мас елементів. | 2. Обчислення за хімічною формулою, пов’язані з поняттям “моль” і законом Авогадро. | 2. Розрахунки маси розчинника і розчиненої речовини для приготування розчину заданої концентрації. |
| 3. Розрахунки за формулою маси елемента по масі речовини. | 3. Розрахунки за хімічними рівняннями. | 3. Знаходження об’ємних співвідношень реагуючих газів. Обчислення відносної густини газів. |
| 4. Розрахунки відносної молекулярної маси за відносною густиною і об’ємом газів за масою речовин. | 4. Виведення формул речовин. | 4. Знаходження відносної молекулярної маси за масою даного об’єму газу і виведенням молекулярної формули речовини. |
| 5. Розрахунки за розчинами. | 5. Періодичний закон і будова атома. | 5. Знаходження практичного виходу речовин. |
| 6. Розрахунки за хімічними рівняннями. | 6. Розчини. | 6. Знаходження кількості речовини, яке буде в продуктах реакції, якщо одна з речовин взята в надлишку. |
| 7. Співставлення найпростіших і молекулярних формул. | 7. Комбіновані задачі з політехнічним змістом. | 7. Знаходження кількості речовини, яке може бути одержаним із вихідної речовини, що містить певний відсоток домішок. |
| 8. Знаходження кількості газоподібних продуктів реакції в об’ємних одиницях виміру. |
При розв’язуванні кількісних задач необхідний глибокий і всебічний якісний аналіз, знаходження хімічної суті задачі. У такому випадку розв’язування кількісних задач буде сприяти глибокому і усвідомленому засвоєнню учнями законів, теорій і понять хімії, формуванню міцних знань, вихованню діалектико-матеріалістичного світогляду учнів.
Виходячи з числа залежностей, які включені в задачу, кількісні хімічні задачі діляться на прості і комбіновані.
Прості задачі потребують нескладного аналізу і незначних математичних розрахунків, які наскільки спрощені, що їх можна розв’язувати усно. Мета розв’язування простих задач – допомогти учням запам’ятовувати формули , конкретизувати одержані знання, закріпити знання від окремих хімічних явищ і фактів.
За дидактичною метою майже всі прості задачі відносяться до тривіальних.
Якщо в задачах використовується кілька закономірностей із різних розділів хімії, а іноді і фізики, то їх називають комбінованими. Такі задачі іноді містять матеріал, який впливає на створення проблемної ситуації. Комбіновані задачі можна використовувати для поглиблення знань учнями, розширення їх бачення про хімічні явища, а також для тематичної перевірки знань учнів. За дидактичною метою майже всі комбіновані задачі відносяться до пізнавальних або розвиваючих.
Вміння розв’язувати прості задачі – необхідні умови для розв’язування складних задач. При наявності такого вміння проблема в тому, щоб знайти сукупність простих задач розв’язання яких призведе до шуканої відповіді. Пошук такої сукупності може відбуватися двома шляхами: синтетичним і аналітичним.
Аналіз задач активізує мислення учнів. Оволодіння аналітико-синтетичними операціями – одна із складних, але в той же час і важливих цілей навчання школярів розв’язуванню хімічних задач. Зрозуміти задачу – значить так чи інакше передбачити її розв’язування, розібратися у тому, що дано і що потрібно знайти. Аналіз задачі важливий для всього процесу розв’язку, так як дає можливість “намітити гіпотезу, як ідею розв’язування задачі (Гаврусейко І.П.)”.
Як показує практика, складності в розв’язуванні задач, обумовлені невмінням аналізувати запропоновану задачу. При систематичному методі аналізу роздуми будуються від змісту задачі до питання, тобто від відомих величин до невідомих, а при аналітичному – від шуканої величини до відомої.

Учитель повинен пояснити учням два способи мислення, щоб можна було використовувати той шлях, який найбільше відповідає їх мисленню. При використанні синтетичного шляху встановлюється, що дано в умові задачі, які величини це дозволяють визначити, що потрібно знайти в кінцевому результаті, чи досить інформації для знаходження шуканої величини.
Якщо ж учню важко встановити зв’язок між відомими і невідомими величинами, то дослідження задачі краще вести аналітичним шляхом, де звертається увага на невідому величину, як її визначити, тобто яке теоретичне положення або закон необхідно для цього використати. Виявивши питання, виділяють прямі і непрямі зв’язки шуканої величини з відомими даними умови задачі.
На практиці при розв’язуванні хімічних задач практично неможливо чітко розділити методи аналізу і синтезу. Вони поєднуються і доповнюються один одним. Аналітичний метод впливає на розвиток продуктивного, логічного і функціонального мислення учнів. Внаслідок систематичного використання аналітичного методу в учнів швидше, ніж при використанні синтетичного, формується вміння самостійно розв’язувати нові для них задачі.
Шляхи розв’язування задач різноманітні. Розв’язування хімічних задач складається з різноманітних і багатьох операцій, які повинні бути конкретних чином взаємопов’язані між собою, використовуватися у певній послідовності, мати певну логіку. Важливим фактором при навчанні розв’язування задач є необхідність обробки деякої послідовності дій. Вона може бути такою (схема 4):
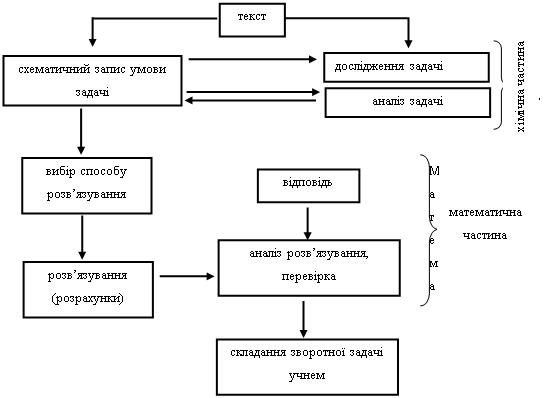 Схема 4
Схема 4
У практиці роботи учителів хімії зустрічаються два способи розв’язування задач. Традиційний спосіб здійснюється за такою схемою: пояснення методів розв’язування – колективне розв’язування – самостійне розв’язування контрольних задач. Іноді колективне розв’язування заміняють самостійною роботою вдома. У цьому випадку ефективність навчання значно знижується.
Другий спосіб відбувається за такою схемою: пояснення шляхів розв’язування задач – колективне розв’язування задач – напівсамостійна робота учнів – самостійна робота – контрольна робота. Методична і навчаюча ефективність цього методу досить висока. На жаль, на практиці роботи вчителів хімії цей метод використовується дуже рідко (С.Г. Шаповаленко).
У методичних посібниках при навчанні вмінню розв’язувати розрахункові задачі, пропонують активно використовувати алгоритми, які допомагають вибирати найбільш раціональний спосіб розв’язування задач, а також прискорюють темпи навчання. При цьому суттєво зменшуються не продуктивні затрати часу на уроці. Цей прийом активізує діяльність учнів, розвиває у них логічне і творче мислення, сприяє виробленню необхідних при розв’язуванні розрахункових задач умінь і навичок.
Таким чином, як свідчить аналіз літератури, розв’язування розрахункових задач – важливий процес навчання хімії. Найкращих результатів можна досягти при систематичному розв’язуванні різноманітних видів задач. Методологічною основою розв’язування розрахункових хімічних задач являється єдність якісної і кількісної сторін хімічних явищ, отже в процесі розв’язування задач важливо обумовити хімічну частину, а потім тільки робити розрахунки.
2.2 Система розрахункових задач для учнів 9 – 11 класів загальноосвітньої школи
Шкільні олімпіади є однією з наймасовіших та найефективніших форм пошуку навчання та виховання учнівської молоді. Роль предметних олімпіад у розвитку творчих здібностей учнів важко переоцінити. Саме на олімпіадах кожний учасник має можливість виявити знання, висловити свою думку, захистити власну ідею, показати навички та вміння дослідницької роботи, адже це і є творчість.
Учнівські олімпіади з базових дисциплін складаються з кількох етапів, але не мають точно визначених початку і кінця. Написання учнями робіт, що власне, прийнято вважати олімпіадою певного етапу – це лише вершина айсберга, основою якого є наполеглива, кропітка праця учнів та їх учителів протягом навчального року. дуже важливим є те, що олімпіади, як і будь-які змагання, захоплюють, змушують долати труднощі в здобутті нових знань та вмінь.
Для дітей, охоплених олімпіадним рухом, наукові змагання стали невід’ємною частиною їхнього повноцінного життя. Вони стимулюють розвиток юної особистості в науковому, інтелектуальному плані, загартовують волю, адже психологічне навантаження під час змагань досить велике. Можна сказати, що олімпіада – це школа життя, де потрібно вміти визнавати стратегію і вибудовувати тактику досягнення перемоги, уміти гідно програвати та робити правильні висновки з поразок.
Завдання хімічних олімпіад потребують не тільки формальних знань і наявності стандартних навиків при розв’язуванні задач, але й умінь творчо використовувати набуті знання для вирішення тих чи інших проблем. Відмітимо особливості олімпіад них задач, які, як правило, являються комплексними, з широким використанням міжпредметних зв’язків., тобто при розв’язуванні необхідно використовувати різноманітні уміння і навички.
Задачі і вправи, які ми пропонуємо, можуть бути використані не тільки при складанні завдань хімічних олімпіад, а навіть при проведенні конкурсів. Більшість задач якісного характеру можна використовувати на практичних заняттях хімічних кружків і при позакласній роботі. Деякі задачі вчитель може використовувати як дидактичний матеріал, особливо при індивідуальній роботі учнів.
Система задач для учнів 8 – 11 класів.
І. Тексти задач для учнів 8 класу.
1. Будова зовнішнього електронного шару атома елемента – 3s23p3. Складіть повну електронну формулу будови цього атома; Визначте якому елементу вона відповідає. Напишіть формулу вищого гідроксиду цього елементу і наведіть два рівняння реакції, які характеризують властивості гідроксиду.
2. Складіть структурні формули вищих оксиду йоду і гідроксиду йоду.
3. Які з перерахованих сполук будуть реагувати з розчином гідроксиду натрію: гашене вапно, оксид стронцію, оксид фосфору (V), сірчана кислота, гідроксид алюмінію? Напишіть рівняння можливих реакцій.
4. Маємо такі речовини: соляна кислота, сіль кухонна, кварц, їдкий натр. За допомогою яких хімічних реакцій їх можна розрізнити.
5. 1 літр вуглекислого газу при нормальних умовах має масу 1,977 г. Який об’єм молю цього газу при нормальних умовах? Відповідь поясніть.
6. На урівноважено дві колби, в яких знаходиться по 100 г 20% соляної кислоти. У одну з них внесли 20 г металічного цинку, в другу – 20 г мармуру. Чи зміниться рівновага по закінченню реакції? Відповідь підтвердіть розрахунками.
7. Мідну пластинку масою 20 г на деякий час опустили у розчин нітрату ртуті (ІІ). Маса пластинки збільшилась на 2,74 г. Потім пластинку нагріли і вона стала початкового кольору. Скільки важить пластинка після нагрівання?
8. При нагріванні водного розчину Н4Р2О7 утворюється ортофосфорна кислота Н3РО4. Розрахуйте концентрацію розчину Н4Р2О7 при нагріванні якого отримуємо 10% розчин Н3РО4.
9. У якому об’ємному співвідношенні потрібно змішати 20%-ний розчин сірчаної кислоти (r=1,14 г/см3) і гідроксиду натрію (r=1,22 г/см3), щоб отримати нейтральний розчин?
10. До 110 г 10%-ної соляної кислоти додали 480 г 5%-ного розчину їдкого натру, а потім добавили ще 367,5 г 8%-ного розчину сірчаної кислоти. Розчин випарували і отриманий сухий осад розігріли до плавлення. Яка вага осаду після нагрівання?
11. У стакан, який містить 200 г 10%-ного розчину соляної і бромоводневої кислот, опустили цинкову пластину. Коли її витягли, промили і висушили, її маса на 6,5 г стала меншою, ніж до реакції. Визначте концентрацію соляної кислоти, яка залишилася в розчині.
12. Для нейтралізації 20 мл розчину соляної і бромоводневої кислот потрібно 50 мл 0,4Н розчину лугу, а при дії на таку ж кількість розчину кислот надлишку розчину солі срібла випало 0,3315 г осаду. Визначте концентрацію кислот у вихідному розчині.
ИНТЕРЕСНОЕ
© 2009 Все права защищены. |